En raison du vieillissement progressif de la population et de l'absence de traitements curatifs, le nombre de personnes souffrant de maladies neurodégénératives a considérablement augmenté au cours des dernières décennies et devrait croître de manière régulière dans les années à venir.
Le développement de nouveaux outils pour modéliser ces pathologies devient donc nécessaire pour aider à comprendre leur physiopathogénie, et trouver rapidement des molécules d'intérêt thérapeutique.
Les organoïdes cérébraux, structures tridimensionnelles dérivées de cellules souches humaines, sont utilisés dans ce cadre pour étudier le développement de certaines maladies neurodégénératives. Des publications récentes ont présenté la pertinence de ce modèle pour l'étude de la maladie d'Alzheimer avec la mise en évidence de marqueurs spécifiques de cette maladie. Cependant, pour assurer une modélisation in vitro rigoureuse, se pose la question de l'utilisation d'échantillons « contrôle » adéquats.
En raison de la multiplicité des facteurs génétiques lors de la comparaison des cellules de deux individus, il faut s'assurer d'avoir des contrôles isogéniques1 adaptés.
Pour créer des modèles d'organoïdes cérébraux isogéniques, l'édition génétique des cellules souches peut être utilisée avec néanmoins, des limites dans leurs applications. L'utilisation de vecteurs rétroviraux (i.e. lentivirus) est quant à elle incompatible avec la modélisation à long terme nécessaire pour ce type d'étude, et comprend un risque d'intégration aléatoire dans le génome hôte. Les méthodes d'ingénierie génétique utilisant CRISPR-Cas9 sont encore trop complexes et coûteuses pour être adaptées en routine aux cellules souches.
C'est dans ce contexte que le laboratoire partenarial SEPIA (CEA/Institut de biologie François Jacob) - CellTechs (Sup'Biotech), en collaboration avec le laboratoire Gly-CRRET (UPEC), a utilisé une stratégie alternative d'ingénierie génétique reposant sur l'utilisation des vecteurs plasmidiques épisomaux pour développer des organoïdes cérébraux isogéniques (contrôles vs pathologiques) pour l'étude d'une forme génétique de démence fronto-temporale.
Les démences fronto-temporales (DFT) constituent un groupe de maladies neurodégénératives caractérisées par des troubles du comportement et du langage, associés à une détérioration intellectuelle. Elles font partie des démences neurodégénératives les plus fréquentes après la maladie d'Alzheimer et sont dues à l'altération progressive des zones frontales et temporales du cerveau.
Il existe certaines formes génétiques de DFT, qui touchent plusieurs membres d'une même famille (formes familiales). Parmi elles, certaines sont dues à une mutation du gène codant pour la protéine tau. La protéine tau s'accumule et forme des inclusions toxiques entraînant la dégradation des neurones. La tauopathie observée est d'autant plus intéressante qu'elle est proche de celle observée dans la maladie d'Alzheimer.
En développant des modèles d'organoïdes cérébraux humains de DFT, il serait donc possible de récapituler les marqueurs du versant tauopathique de la maladie d'Alzheimer qui sont :
une perte synaptique ,
une hyperphosphorylation de la protéine tau,
l'apparition de dégénérescences neurofibrillaires,
la mort neuronale.
Pour cela, les chercheurs ont modifié génétiquement des cellules souches pluripotentes induites humaines en utilisant des plasmides épisomaux dérivés du virus Epstein-Barr. Ces plasmides permettent l'expression d'un transgène dans la cellule et sont capables de se répliquer durant la division cellulaire grâce à la présence d'une origine de réplication sur l'épisome, sans intégration dans le génome hôte. Le maintien du plasmide comme élément extra-chromosomique en faible copie est possible grâce à la séquence génétique EBNA-1, et son maintien dans la cellule est réalisé par sélection en ajoutant des antibiotiques en culture.
Deux lignées de cellules souches isogéniques ont été créées à partir d'une même lignée contrôle : une lignée surexprimant une forme normale du gène codant pour la protéine tau et une lignée surexprimant la forme mutée (P301S) de ce même gène.
La protéine tau (normale vs mutée) surexprimée est de plus, couplée à un rapporteur fluorescent permettant de s'assurer du suivi du maintien du plasmide épisomal dans la cellule. Ces lignées expriment de manière stable, et ce, pendant plus de 30 passages, les formes génétiques décrites.
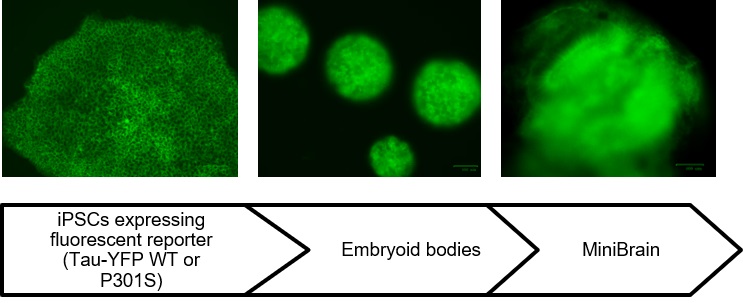
Cellules souches induites pluripotentes humaines exprimant la protéine tau couplée à un rapporteur fluorescent grâce à un vecteur épisomal, différenciées en corps embryoïdes et organoïdes cérébraux. (crédit photo : F. Nassor)
Des organoïdes cérébraux ont été obtenus à partir de ces lignées, la présence des plasmides dans les cellules n'interférant pas avec le protocole de différenciation.
De plus, les organoïdes porteurs de la mutation génétique présentent un profil d'hyperphosphorylation pathologique de la protéine tau similaire au début du processus pathologique observé chez l'humain atteint de la DFT.
Cette nouvelle approche permet de montrer la faisabilité technique de l'expression d'un transgène dans les cellules souches humaines de façon simple et efficace sans pour autant entraver les protocoles de différenciation nécessaire à l'étude plus poussée de pathologies. Dans le cadre de cette étude, les auteurs ont pu montrer que l'organoïde cérébral était en mesure de développer les premières étapes de la DFT dans un modèle d'étude complexe humain. Cette méthodologie pourra à terme être utilisée pour d'autres pathologies génétiques afin de créer des modèles isogéniques.
Un tel système, simple de conception et polyvalent, ouvre un nouveau potentiel dans l'utilisation des cellules souches et des organoïdes humains pour la modélisation in vitro, la médecine personnalisée et l'expérimentation de nouvelles thérapeutiques.
1 : Dans une lignée isogénique tous les individus partagent le même patrimoine génétique, ce qui permet de les comparer facilement entre eux. Ainsi lorsqu'un gène est remplacé par un autre et que l'on peut observer une nouvelle particularité, il est donc possible d'attribuer la modification à ce nouveau gène.
Ces travaux de recherche ont été soutenus financièrement par le Programme Investissement d'Avenir PIA2 n° P112331-3422142 (projet 3DNS), le programme européen JPND (3DMiniBrain) et la fondation ANS.