Une expertise étendue
Les modèles dans la recherche en biologie santé
Dans le domaine de la biologie-santé, un modèle représente un objet (cellule, organe, organisme) ou un processus (fonctions physiologiques [digestion, respiration, …], évolution d’une maladie, réactions d’un organisme, …) qui remplace l’objet ou le processus original pour l’étudier de façon contrôlée et sans risques pour l’être humain.
Le fonctionnement des êtres vivants est très complexe. Comprendre les pathologies humaines et développer de nouvelles thérapies nécessitent de les explorer à différents niveaux d’organisation : molécule, cellule, organe, individu.
Les études sur les premiers niveaux d’organisation (cellules ou des assemblages de cellules) peuvent être réalisées en dehors de l'organisme, dans des éprouvettes par exemple. C'est la recherche in vitro.
Une partie du fonctionnement d'une cellule ou d'un organe peut être étudiée sur ordinateur (modélisation informatique). On parle alors de recherche in silico.
Pour étudier les processus les plus complexes et reproduire les interactions multiples au sein d'un organisme vivant, l'utilisation des animaux est une pratique scientifique indispensable. Il s'agit alors de la recherche in vivo. Dans le cas des maladies infectieuses par exemple, la complexité d'une infection virale ou de la réponse immunitaire ne peut pas être reproduite par un modèle in vitro ne représentant que partiellement un organisme.
Qu’est-ce qu’un modèle animal ?
C’est une représentation chez l’animal d’un processus biologique normal ou pathologique chez l'humain. La caractérisation de cette représentation, sa capacité à "mimer" le processus chez l'humain et sa pertinence pour le développement de traitements ou de vaccins font l’objet de travaux scientifiques approfondis.
Cette pertinence est fondée, comme pour tout modèle expérimental, sur la similitude chez le modèle et chez l'humain, des mécanismes impliqués dans le processus étudié, depuis la cause jusqu’à l’expression des effets. Les programmes faisant appels aux modèles in vivo font l’objet d’une double validation : celle de comités d’experts scientifiques, et celle des comités d’éthique et du Ministère de l’Enseignement supérieur, de la Recherche et de l’Innovation.
Il permet de mieux comprendre certaines pathologies humaines difficiles à étudier autrement.
C’est souvent un animal présentant une pathologie comparable à celle observée chez l'humain et apparue de façon naturelle (modèle spontané) ou induite (infection par un virus, intervention chirurgicale, modification d’un gène, utilisation d’un produit chimique).
Il permet aussi de mieux comprendre le fonctionnement des organes sains, en dehors de toute pathologie, préalable nécessaire à une meilleure compréhension des maladies.
Chikungunya
L'absence de traitement spécifique conduit à s'intéresser à des molécules qui présentent une activité antivirale in vitro. Chacune d’elles doit être testée pour en déterminer les avantages et les inconvénients. Le développement d'un modèle animal d'infection et des résultats obtenus chez une cohorte de patients a permis de montrer que la chloroquine favorise la réplication du virus dans l'organisme et retarde la mise en place de l'immunité adaptative, écartant de fait son utilisation en clinique.
Les équipes d'IDMIT ont participé à des études précliniques pour valider le passage en phase clinique III d'un vaccin vivant atténué ne nécessitant qu'une seule injection qui a induit des anticorps chez 100% des patients sains inclus dans la phase I de l'étude clinique. IDMIT a pu vérifier l'absence de persistante du virus vaccinal à long terme -donc le risque d'induction de pathologie associé- et démontrer son efficacité contre l'infection.
Chlamydiose
La bactérie Chlamydia trachomatis peut induire, d’une part une infection oculaire responsable du trachome (conjonctivite chronique), et d’autre part, une infection sexuellement transmissible souvent asymptomatique mais dont les conséquences peuvent être sévères en absence de traitement : inflammation des muqueuses génitales, de la gorge, des paupières, infertilité chez la femme. Dans le cadre de projets européens, IDMIT participe à l'identification d'un vaccin qui contrôle l'infection vaginale et l'infection oculaire chez un modèle animal. Ce vaccin est en cours d'évaluation dans des essais cliniques.
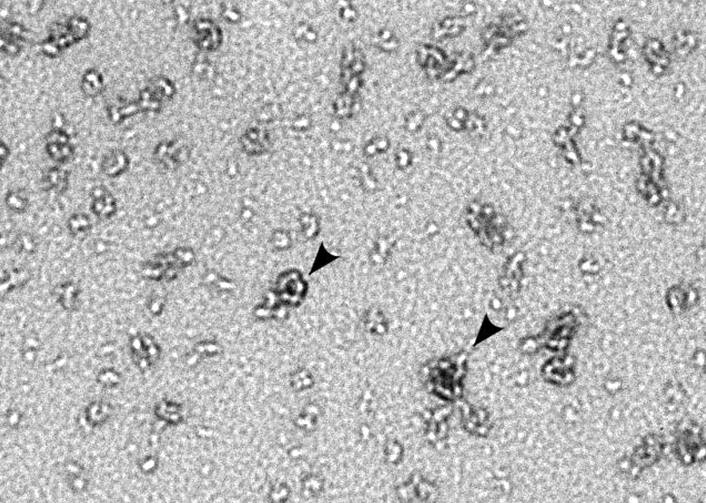
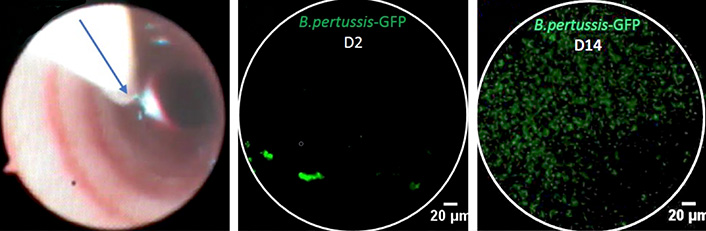
Coqueluche
Une équipe d'IDMIT a mis au point un modèle animal d'infection par la bactérie responsable de la coqueluche. Une méthode de détection de la bactérie dans l'organisme par imagerie in vivo a ainsi pu être validée, permettant de caractériser la maladie et son évolution. D'importants projets sont réalisés dans le cadre de programmes européens et en partenariat avec des industriels pour tester différentes technologies de vaccins. L'objectif est de prévenir l'apparition de la maladie chez les très jeunes enfants.
Les méthodes d'imagerie validées dans le cadre de ces études sur la coqueluche sont maintenant utilisées pour l'étude d'autres maladies.
Voir la fiche d’identitéFièvre jaune
Le vaccin contre la fièvre jaune est l’un des plus efficaces qui existe : une seule infection permet de protéger l’individu vacciné pendant au moins dix ans. Comprendre les mécanismes moléculaires et cellulaires qui expliquent la durabilité remarquable de ce vaccin permettrait sans aucun doute d’améliorer des vaccins contre d’autres pathogènes et de donner les clés pour lutter contre des pandémies majeures comme le SIDA ou la tuberculose.
Les chercheurs d'IDMIT étudient ces mécanismes précoces, induits par la vaccination contre la fièvre jaune. L'objectif est d'analyser la réponse immunitaire à la vaccination pour dégager des signatures immunitaires qui corrèlent avec la production d'anticorps à très long terme. À partir de ces données, les chercheurs développent des modèles mathématiques qui permettront de prédire très tôt l'efficacité d'un vaccin sur le long terme, rien qu'en étudiant la réponse précoce. Ils étudient également la manière dont ces mécanismes pourraient être sollicités pour de nouvelles générations de vaccins contre différents types de pathogènes.
Voir la fiche d’identité

Grippe saisonnière
Chez les personnes à risque, les complications de la grippe sont souvent dues à des infections bactériennes, principalement au niveau des poumons. Les chercheurs d’IDMIT étudient les mécanismes qui favoriseraient ces co-infections. Ils cherchent par ailleurs à comprendre les mécanismes des pneumonies graves, évaluent l'efficacité de vaccins à ADN et ARN messager et de nouvelles stratégies de vaccins qui assureraient une protection sur plusieurs années vis-à-vis d'un spectre large de souches du virus.
Nouvelles souches, nouveaux variants, comment s'adapter ?
Lorsque le virus se réplique dans les cellules infectées, certaines des copies produites peuvent contenir des erreurs : on parle de mutation. Si tous les virus peuvent muter, on sait que les virus à ARN (comme le SARS-CoV-2 responsable de la Covid-19 et les virus de la grippe) sont plus sujets aux mutations. Une mutation peut entraîner l'émergence d'une nouvelle souche, alors appelée variant.

Différentes souches peuvent circuler, simultanément ou non, pour un même virus : par exemple les souches A(H1N1) et A(H5N1) pour le virus de la grippe A, ou les variants alpha et delta pour le SARS-CoV-2.
Les traitements et vaccins peuvent s'avérer plus ou moins efficaces contre les différentes souches.
Le vaccin contre la grippe change tous les ans
Des souches différentes de virus de la grippe peuvent circuler chaque année. En outre, l'immunité diminue avec le temps. Les vaccins contre la grippe saisonnière sont mis à jour tous les ans afin d'assurer la meilleure protection possible en veillant à les faire correspondre au mieux aux virus en circulation. Leur efficacité ne peut pas être connue avant la période épidémique.
Variants du SARS-CoV-2 et vaccins contre la Covid-19
Lors de l'émergence d'un nouveau variant, l'efficacité des vaccins existant est évaluée en suivant les mêmes étapes que pour le développement d'un vaccin. Dans le cas de la Covid-19, la vaccination à large échelle et sa surveillance étroite permettent d'obtenir rapidement des données en conditions réelles. Si les vaccins s'avéraient inefficaces contre de nouveaux variants, alors un nouveau vaccin devrait être développé. La technologie des vaccins à ARN messager permettrait une adaptation rapide et contrôlée.
Lutte contre la menace bioterroriste
En 2005, l'État a confié au CEA la responsabilité d'un programme interministériel de recherche et développement contre les risques terroristes, avec une priorité donnée aux menaces NRBC-E (nucléaire, radiologique, biologique, chimique et explosif).
L'infrastructure IDMIT a rejoint ce programme en 2015. Quel est le rapport entre la lutte contre le terrorisme et les maladies émergentes ou réémergentes ? Les mêmes agents pathogènes, qui peuvent être des virus ou des toxines. IDMIT développe des modèles animaux pour caractériser l'infection par de tels agents aux niveaux physiopathologique, métabolique et cellulaire. L'objectif est de prédire ce qui pourrait se passer chez l'humain pour proposer et valider des solutions thérapeutiques en termes de traitements et de prévention.
Maladies auto-immunes
Les maladies auto-immunes sont dues à un dérèglement du système immunitaire, qui se retourne contre son propre organisme. Face à ces maladies, le développement de stratégies s'avère complexe : il s'agit de ne pas affaiblir le système immunitaire en cas d'agression par des pathogènes extérieurs tout en limitant les réactions auto-immunes. Les équipes d'IDMIT étudient les mécanismes moléculaires liés à ces maladies, pour envisager de nouvelles stratégies thérapeutiques chez les malades.
Les équipes d’IDMIT travaillant au Centre Hospitalier Universitaire de Bicêtre ont notamment identifié une cible intéressante pour traiter le syndrome de Sjögren primitif, caractérisé par une diminution des sécrétions de larmes et de salive, mais qui peut toucher d'autres organes (poumons, reins). Elles recherchent également de nouvelles cibles pour traiter la polyarthrite rhumatoïde, la maladie auto-immune systémique la plus fréquente, qui provoque une inflammation chronique et déformante des articulations.
Microbiotes et maladies infectieuses
Le microbiote est impliqué dans le développement du système immunitaire et l'efficacité de la réponse immunitaire. Il est fragile et peut être perturbé par des modifications de l'environnement, des maladies, des traitements. Chez les personnes bien portantes, le retour à la normale est généralement rapide. Les chercheurs d’IDMIT étudient la composition du microbiote et ses évolutions dans le cadre de plusieurs maladies et cherchent à savoir comment un dérèglement du microbiote pourrait être associé à une plus forte susceptibilité face à certaines infections. Les projets en cours concernent particulièrement :
- le microbiote vaginal :
- influence d'une dérégulation sur le risque d'infection par le VIH (et notamment en cas de co-infection à Chlamydia)
- variations au cours du cycle menstruel et caractérisation des molécules et cellules immunitaires
- perturbation par le liquide séminal
- le microbiote intestinal :
- perturbation suite à une infection (VIH, SARS-CoV-2) et influence des traitements sur son évolution. Les chercheurs d'IDMIT ont montré qu'une infection par le SARS-CoV-2 modifie durablement la composition du microbiote intestinal.
- influence sur les mécanismes de l'infection et de l'inflammation
- le microbiote pulmonaire : caractérisation et évolution en cas d'infections respiratoires (grippe, Covid-19).
Les chercheurs d'IDMIT s'intéressent également au rôle des différents microbiotes dans le développement et la maturation du système immunitaire.


Paludisme
Les équipes d'IDMIT étudient des combinaisons de molécules pour augmenter l'efficacité des médicaments actuellement disponibles sur les formes actives et dormantes du parasite causant le paludisme. Ils ont développé des protocoles pour la culture ex vivo des formes actives et dormantes du parasite, qui confirment les résultats obtenus chez les patients et les modèles animaux et qui pourraient guider l'élaboration de nouvelles voies thérapeutiques.
Recherche vaccinale
Le département IDMIT participe à plusieurs programmes de développement de nouveaux vaccins contre différentes maladies. Il développe aussi des projets de recherches plus fondamentaux pour améliorer la connaissance des mécanismes moléculaires et cellulaires du processus d’immunisation afin d’améliorer les stratégies de vaccination (affiner les calendriers vaccinaux par exemple) et identifier les facteurs clés qui permettront de concevoir de nouvelles approches vaccinales.
IDMIT cherche à affiner l'utilisation de vecteurs, adjuvants et modes d'administration et développe de nouveaux outils pour améliorer la surveillance en temps réel de la réponse immunitaire. Un des objectifs est d'identifier de nouveaux biomarqueurs qui pourraient être facilement transposables à l'humain.
Décrypter les réponses immunitaires pour affiner le calendrier vaccinal
Le dogme selon lequel les cellules de l'immunité innée seraient dépourvues de "mémoire" est aujourd'hui remis en question. Alors que la vaccination se base sur la réponse immunitaire adaptative, des travaux menés à IDMIT montrent que les réponses des cellules immunitaires innées sont différentes entre une première vaccination et les rappels… La modulation des réponses innées de rappel pourrait aider à augmenter l’efficacité et la durabilité de la mémoire vaccinale.

Zika
En collaboration avec l’Institut Pasteur, IDMIT participe à un consortium qui vise à mettre au point un vaccin contre le virus Zika en utilisant un virus inactivé de la rougeole comme vecteur. Ce type de vecteur a déjà montré son efficacité avec des preuves de concept confirmées sur une variété de pathogènes.
Les chercheurs s'intéressent aussi à identifier des traitements de prévention efficaces ainsi qu'à l'étude de la physiopathologie de la transmission du virus. Ils ont montré qu'un métabolite d'un insecticide largement utilisé au Brésil avait un effet sur la maturation du système nerveux central et donc pouvait expliquer le nombre exceptionnellement élevé de microcéphalies là où ce produit est distribué dans l’eau potable pour diminuer la prolifération des moustiques. Enfin, ils étudient la transmission du virus in utero de la mère à l'enfant pour déterminer les voies et sites principaux atteints par le virus et donc les cibles potentielles d’un traitement.